细胞与细胞之间的连接有哪些方式,常见的细胞连接方式有哪几种
发布:小编
本文目录
常见的细胞连接方式有哪几种
1、紧密连接(tight junction)
也称闭锁小带(zonula occludens)。这种连接为点状,斑状或带状,常见的为带状。位于细胞(如上皮细胞)的顶端,呈箍状围绕细胞。相邻细胞间的顶部细胞间隙被封闭,相邻细胞膜表面有呈网状的嵴,嵴与嵴相连处细胞膜紧贴而封闭细胞间隙,这种连接除有机械性的连接作用处,并封闭了细胞顶端的细胞间隙,可阻止大分子物质由外部进入细胞间隙,在胃肠道的上皮细胞顶部就广泛存在着这种连接。
2、中间连接(intermediate junction)
也称粘着小带(zonula adherens)。此种连接多为长短不一的带状,将细胞粘着在一起,相邻邦细胞间有宽约 15-20 nm 的间隙,内充满密度较低的均质性物质。在细胞膜的胞质面,附着有薄层致密物质和微丝,粗约 5 nm ,一端附着于细胞膜的内层,另一端在细胞质内交织成网(终末网)。这种连接多见于上皮和心肌细胞。
3、桥粒(desmosome)
也称粘着斑(macula adherens)。呈长型小盘状大小不等,此处细胞间隙宽约 20-30 nm ,其中充满低密度的物质,中间有一致密的中线由丝状物质交织而成。细胞膜内侧有深暗的致密的较厚的板状结构,称为附着板(attachment plaqne)。胞质中有许多直径 10 nm 袢状张力丝(tonofilament),附着其上,起一定的支持作用。桥粒的连接甚为牢固,多分布于易机械性刺激和磨擦较多的地方。某些上皮细胞的基底与深部结缔组织的相邻面,有半桥粒的结构,将上皮固着于基膜上。
4、缝管连接(gap junction)
斑状,细胞间隙为 2-3 nm ,相邻邦细胞膜间有间隔大致相等的连接点。连接点处细胞膜上有小管相通连,使相邻细胞相通,供细胞间交换离子,小分子物质(荧光素等)相邻细胞间交换化学信息,此种连接处电阻低,易进行离子交换和传递电冲动,此种连接分布较广,上皮、肌细胞、骨细胞和神经细胞之间都有。
细胞靠什么连接在一起
细胞与细胞间或细胞与细胞外基质的联结结构称为细胞连接(cell junction).细胞连接的体积很小,只有在电镜下才能观察到.可分为三大类,即:封闭连接(occluding junction)、锚定连接(anchoring junction)和通讯连接(communicating junction).
第一节 细胞连接
一、封闭连接
(一)紧密连接(tight junction)
又称封闭小带(zonula occludens),存在于脊椎动物的上皮细胞间(图11-1),长度约50-400nm,相邻细胞之间的质膜紧密结合,没有缝隙.在电镜下可以看到连接区域具有蛋白质形成的焊接线网络,焊接线也称嵴线(图11-2,3),封闭了细胞与细胞之间的空隙.上皮细胞层对小分子的透性与嵴线的数量有关,有些紧密连接甚至连水分子都不能透过.
紧密连接的焊接线由跨膜细胞粘附分子构成,主要的跨膜蛋白为claudin和occludin,另外还有膜的外周蛋白ZO.
紧密连接的主要作用是封闭相邻细胞间的接缝,防止溶液中的分子沿细胞间隙渗入体内,从而保证了机体内环境的相对稳定;消化道上皮、膀胱上皮、脑毛细血管内皮以及睾丸支持细胞之间都存在紧密连接.后二者分别构成了脑血屏障和睾血屏障,能保护这些重要器官和组织免受异物侵害.在各种组织中紧密连接对一些小分子的密封程度有所不同,例如小肠上皮细胞的紧密连接对Na+的渗漏程度比膀胱上皮大1万倍.
图11-1紧密连接位于上皮细胞的上端
图11-2兔子上皮细胞的紧密连接(冰冻蚀刻)
图11-3 紧密连接的模式图
(二)间壁连接(septate junctions)
是存在于无脊椎动物上皮细胞的紧密连接(图11-4).连接蛋白呈梯子状排列,形状非常规则,连接的细胞内骨架成分为肌动蛋白纤维.在果蝇中一种叫做discs-large的蛋白参与形成间壁连接,突变品种不仅不能形成间壁连接,还产生瘤突.
图11-4 间壁连接存在于无脊椎动物
二、锚定连接
(一)粘合带与粘合斑
粘合带(adhesion belt)呈带状环绕细胞,一般位于上皮细胞顶侧面的紧密连接下方(图11-5).在粘合带处相邻细胞的间隙约15~20nm.
图11-5 粘合带位于紧密连接下方
间隙中的粘合分子为E-钙粘素(图11-6).在质膜的内侧有几种附着蛋白与钙粘素结合在一起,这些附着蛋白包括:α-,β-,γ-连锁蛋白(catenin)、粘着斑蛋白(vinculin)、α-辅肌动蛋白(α-actinin)和片珠蛋白(plakoslobin).
图11-6 粘合带结构模型
粘合带处的质膜下方有与质膜平行排列的肌动蛋白束,钙粘蛋白通过附着蛋白与肌动蛋白束相结合.于是,相邻细胞中的肌动蛋白丝束通过钙粘蛋白和附着蛋白编织成了一个广泛的网络,把相邻细胞联合在一起.
粘合斑(adhesion plaque)位于细胞与细胞外基质间,通过整合素(integrin)把细胞中的肌动蛋白束和基质连接起来.连接处的质膜呈盘状,称为粘合斑.
(二)桥粒与半桥粒
桥粒(desmosome)存在于承受强拉力的组织中,如皮肤、口腔、食管等处的复层鳞状上皮细胞之间和心肌中(图11-7).相邻细胞间形成纽扣状结构,细胞膜之间的间隙约30nm,质膜下方有细胞质附着蛋白质,如片珠蛋白(plakoglobin)、桥粒斑蛋白(desmoplakin)等,形成一厚约15~20nm的致密斑.斑上有中间纤维相连,中间纤维的性质因细胞类型而异,如:在上皮细胞中为角蛋白丝(keratin filaments),在心肌细胞中则为结蛋白丝(desmin filaments).桥粒中间为钙粘素(desmoglein及desmocollin).因此相邻细胞中的中间纤维通过细胞质斑和钙粘素构成了穿胞细胞骨架网络(图11-8).
图11-7 桥粒位于粘合带下方
图11-8 桥粒的结构模型
半桥粒(hemidesmosome)在结构上类似桥粒,位于上皮细胞基面与基膜之间(图11-9),它桥粒的不同之处在于:①只在质膜内侧形成桥粒斑结构,其另一侧为基膜;②穿膜连接蛋白为整合素(integrin)而不是钙粘素,整合素是细胞外基质的受体蛋白;③细胞内的附着蛋白为角蛋白(keratin).
图11-9 半桥粒连接上皮细胞基面和基膜
三、通讯连接
(一)间隙连接
间隙连接(gap junction) 存在于大多数动物组织.在连接处相邻细胞间有2~4nm的缝隙(图11-10),而且连接区域比紧密连接大得多,最大直径可达0.3μm.在间隙与两层质膜中有大量蛋白质颗粒,是构成间隙连接的基本单位,称连接子(connexon),由6个相同或相似的跨膜蛋白亚单位环绕而成,直径8nm,中心形成一个直径约1.5nm的孔道(图11-11).通过向细胞内注射分子量不同的染料,证明间隙连接的通道可以允许分子量小于1.5KD的分子通过.这表明细胞内的小分子,如无机盐离子、糖、氨基酸、核苷酸和维生素等有可能通过间隙连接的孔隙.
间隙连接的通透性是可调节的.在实验条件下,降低细胞PH值,或升高钙离子浓度均可降低间隙连接的通透性.当细胞破损时,大量钙离子进入,导致间隙连接关闭,以免正常细胞受到伤害.
图11-10 间隙连接电镜照片
图11-11 左,连接子电镜照片;右,间隙连接模型
间隙连接的功能包括:
1.参与细胞分化:胚胎发育的早期,细胞间通过间隙连接相互协调发育和分化.小分子物质即可在一定细胞群范围内,以分泌源为中心,建立起递变的扩散浓度梯度,以不同的分子浓度为处于梯度范围内的细胞提供”位置信息”(positional information),从而诱导细胞按其在胚胎中所处的局部位置向着一定方向分化.
2.协调代谢:例如,在体外培养条件下,把不能利用外源次黄嘌呤合成核酸的突变型成纤维细胞和野生型成纤维细胞共同培养,则两种细胞都能吸收次黄嘌呤合成核酸.如果破坏细胞间的间隙连接,则突变型细胞不能吸收次黄嘌呤合成核酸.
3、构成电紧张突触:平滑肌、心肌、神经末梢间均存在的这种间隙连接,称为电紧张突触(electrotonic synapses).电紧张突触无须依赖神经递质或信息物质即可将一些细胞的电兴奋活动传递到相邻的细胞.
(二)胞间连丝
胞间连丝(plasmodesmata)是植物细胞特有的通讯连接.是由穿过细胞壁的质膜围成的细胞质通道,直径约20~40nm.因此植物体细胞可看作是一个巨大的合胞体(syncytium).通道中有一由膜围成的筒状结构,称为连丝小管(desmotubule).连丝小管由光面内质网特化而成,管的两端与内质网相连.连丝小管与胞间连丝的质膜内衬之间,填充有一圈细胞质溶质(cytosol).一些小分子可通过细胞质溶质环在相邻细胞间传递(图11-12).
图11-12 胞间连丝结构模型
胞间连丝在功能上与动物细胞间的间隙连接类似,它允许分子量小于800Da的分子通过,在相邻细胞间起通讯作用.但通过胞间连丝的分子运输也要受到调节.实验证明,在胞间连丝正常的情况下,有些低分子量的染料分子却不能通过.然而某些植物病毒能制造特殊的蛋白质,这种蛋白质同胞间连丝结合后,可使胞间连丝的有效孔径扩大,使病毒粒子得以通过胞间连丝在植物体内自由播散和感染.
胞间连丝还对细胞分化起一定作用.在高等植物中,顶端分生组织的细胞分化与胞间连丝的分布有着相应的关系.随着细胞的生长和延长,侧壁上的胞间连丝逐渐减少,而横壁上的却仍保持很多.植物相邻细胞间的细胞核可经胞间连丝穿壁.
(三)化学突触
化学突触(synapse)是存在于可兴奋细胞间的一种连接方式,其作用是通过释放神经递质来传导兴奋.由突触前膜(presynaptic membrane)、突触后膜(postsynaptic membrane)和突触间隙(synaptic cleft)三部分组成(图11-13、14).
图11-13 化学突触的结构(具有小囊泡的一侧为突触前膜)
突触前神经元的突起末梢膨大呈球形,称突触小体(synaptic knob).突触小体贴附在突触后神经元的胞体或突起的表面形成突触.突触小体的膜称突触前膜,与突触前膜相对的胞体膜或突起的膜称突触后膜,两膜之间称为突触间隙.间隙的宽度约20-30nm,内含有粘多糖和糖蛋白等物质.
突触小体内有许多囊泡,称突触小泡(synaptic vesicle),内含神经递质.当神经冲动传到突触前膜,突触小泡释放神经递质,为突触后膜的受体接受(配体门通道),引起突触后膜离子通透性改变,膜去极化或超极化.
图11-14 化学突触的结构模型
表10-1各种连接的比较
封闭连接
紧密连接
上皮组织
间壁连接
只存在于无脊椎动物中
锚定连接
连接肌动蛋白
粘合带
上皮组织
粘合斑
上皮细胞基部
连接中间纤维
桥粒
心肌、表皮
半桥粒
上皮细胞基部
通讯连接
间隙连接
大多数动物组织中
化学突触
神经细胞间和神经—肌肉间
胞间连丝
植物细胞间
图11-15 几类细胞连接的比较
第二节 细胞粘附分子
细胞粘附分子(cell adhesion molecule,CAM)是参与细胞与细胞之间及细胞与细胞外基质之间相互作用的分子.可大致分为五类:钙粘素、选择素、免疫球蛋白超家族、整合素及透明质酸粘素.
细胞粘附分子都是跨膜糖蛋白,分子结构由三部分组成:①胞外区,肽链的N端部分,带有糖链,负责与配体的识别;②跨膜区,多为一次跨膜;③胞质区,肽链的C端部分,一般较小,或与质膜下的骨架成分直接相连,或与胞内的化学信号分子相连,以活化信号转导途径.
多数细胞粘附分子的作用依赖于二价阳离子,如Ca2+,Mg2+.细胞粘附分子的作用机制有三种模式(图11-16):两相邻细胞表面的同种CAM分子间的相互识别与结合(亲同性粘附);两相邻细胞表面的不同种CAM分子间的相互识别与结合(亲异性粘附);两相邻细胞表面的相同CAM分子借细胞外的连接分子相互识别与结合.
图11-16 细胞粘附分子的作用方式
一、钙粘素
钙粘素(cadherin)属亲同性CAM,其作用依赖于Ca2+.至今已鉴定出30种以上钙粘素(表10-2),分布于不同的组织.
图11-17 钙粘素结构模型
钙粘素分子结构同源性很高,其胞外部分形成5个结构域,其中4个同源,均含Ca2+结合部位(图11-17).决定钙粘素结合特异性的部位在靠N末端的一个结构域中,只要变更其中2个氨基酸残基即可使结合特异性由E-钙粘素转变为P-钙粘素.钙粘素分子的胞质部分是最高度保守的区域,参与信号转导.
钙粘素通过不同的连接蛋白质与不同的细胞骨架成分相连,如E-钙粘素通过α-、β-、γ-连锁蛋白(catenin)以及粘着斑蛋白(vinculin)、锚蛋白、α辅肌动蛋白等与肌动蛋白纤维相连;桥粒中的desmoglein及desmocollin则通过桥粒致密斑与中间纤维相连.
表10-2 哺乳动物细胞表面的主要钙粘素分子
名称
主要分布组织
E-钙粘素
着床前的胚胎、上皮细胞(在带状粘合处特别集中)
P-钙粘素
胎盘滋养层细胞、心、肺、小肠
N-钙粘素
胚胎中胚层、神经外胚层、神经系统(脑、神经节)、心、肺
M-钙粘素
成肌细胞、骨骼肌细胞
R-粘素
视网膜神经细胞、神经胶质细胞
Ksp-钙粘素
肾
OB-钙粘素
成骨细胞
VB-钙粘素
脉管内皮细胞
desmoglein
桥粒
desmocollin
桥粒
钙粘素的作用主要有以下几个方面:
1.介导细胞连接,在成年脊椎动物,E-钙粘素是保持上皮细胞相互粘合的主要CAM,是粘合带的主要构成成分.桥粒中的钙粘素就是desmoglein及desmocollin.
2.参与细胞分化,钙粘素对于胚胎细胞的早期分化及成体组织(尤其是上皮及神经组织)的构筑有重要作用.在发育过程中通过调控钙粘素表达的种类与数量可决定胚胎细胞间的相互作用(粘合、分离、迁移、再粘合),从而通过细胞的微环境,影响细胞的分化,参与器官形成过程.
3.抑制细胞迁移,很多种癌组织中细胞表面的E钙粘素减少或消失,以致癌细胞易从瘤块脱落,成为侵袭与转移的前提.因而有人将E钙粘素视为转移抑制分子.
二、选择素
选择素(selectin)属亲异性CAM,其作用依赖于Ca2+.主要参与白细胞与脉管内皮细胞之间的识别与粘合.已知选择素有三种:L选择素、E选择素及P选择素(图11-18).
图11-18 选择素结构模型
选择素的胞外区由三个结构域构成:N端的C型凝集素结构域,EGF样结构域、重复次数不同的补体结合蛋白结构域;通过凝集素结构域来识别糖蛋白及糖脂分子上的糖配体.
E选择素及P选择素所识别与结合的糖配体为唾液酸化及岩藻糖化的N乙酰氨基乳糖结构(sLeX及sLeA).sLeA结构存在于髓系白细胞表面(其中包括L选择素)分子中.多种肿瘤细胞表面也存在sLeX及sLeA结构.
P选择素贮存于血小板的α颗粒及内皮细胞的Weibel-Palade小体.炎症时活化的内皮细胞表面首先出现P选择素,随后出现E选择素.它们对于召集白细胞到达炎症部位具有重要作用.
E选择素存在于活化的血管内皮细胞表面.炎症组织释放的白细胞介素I(IL-1)及肿瘤坏死因子(TNF)等细胞因子可活化脉管内皮细胞,刺激E选择素的合成.
L选择素广泛存在于各种白细胞的表面,参与炎症部位白细胞的出脉管过程.白细胞表面L选择素分子上的sLeA与活化的内皮细胞表面的P选择素及E选择素之间的识别与结合,可召集血液中快速流动的白细胞在炎症部位的脉管内皮上减速滚动(即通过粘附、分离、再粘附……,如此循环往复),最后穿过血管进入炎症部位.
三、免疫球蛋白超家族
免疫球蛋白超家族(Ig-superfamily,Ig-SF)包括分子结构中含有免疫球蛋白(Ig)样结构域的所有分子,一般不依赖于Ca2+.免疫球蛋白样结构域系指借二硫键维系的两组反向平行β折叠结构(图11-19).
图11-19 Ig-SF的结构模型
除免疫球蛋白外,还包括T细胞受体,B细胞受体,MHC及细胞粘附分子(Ig-CAM)等.有的属于亲同性CAM,如各种神经细胞粘附分子(N-CAM)及血小板-内皮细胞粘附分子(Pe-CAM);有的属于亲异性CAM,如细胞间粘附分子(I-CAM)及脉管细胞粘附分子(V-CAM)等.I-CAM及V-CAM的配体都是整合素.
N-CAM有20余种异型分子,它们在神经发育及神经细胞间相互作用上有重要作用.
I-CAM及V-CAM在活化的血管内皮细胞表达.炎症时,活化的内皮细胞表面的I-CAM可与白细胞表面的αLβ2及巨噬细胞表面的αMβ2相结合;V-CAM则可与白细胞的α4β1整合素相结合.它们继上述选择素介导的白细胞与内皮细胞的粘合作用之后使在内皮上滚动的白细胞固着于炎症部位的脉管内皮,并发生铺展,进而分泌水解酶而穿出脉管壁.
四、整合素
整合素(integrin)大多为亲异性细胞粘附分子,其作用依赖于Ca2+.介导细胞与细胞间的相互作用及细胞与细胞外基质间的相互作用(图11-20).几乎所有动植物细胞均表达整合素.
图11-20 整合素结构模型
整合素是由α (120~185kD)和β(90~110kD)两个亚单位形成的异二聚体.迄今已发现16种α亚单位和9种β亚单位.它们按不同的组合构成20余种整合素.
α亚单位的N端有结合二价阳离子的结构域,胞质区近膜处都有一个非常保守的KXGFFKR序列,与整合素活性的调节有关.
含β1亚单位的整合素主要介导细胞与细胞外基质成分之间的粘附.含β2亚单位的整合素主要存在于各种白细胞表面,介导细胞间的相互作用.β3亚单位的整合素主要存在于血小板表面,介导血小板的聚集,并参与血栓形成.除β4可与肌动蛋白及其相关蛋白质结合,α6β4整合素以层粘连蛋白为配体,参与形成半桥粒(图11-21).
图11-21 半桥粒处的α6β4整合素
五、透明质酸粘素
透明质酸粘素(hyaladherin)包括可结合透明质酸糖链的一类分子,具有相似的氨基酸序列和空间构象.CD44族是其中的一个成员,分子量范围为85 KD~250KD,介导细胞与细胞间及细胞与细胞外基质间的相互作用,同样是由胞外,跨膜及胞质三个部分构成的糖蛋白,糖链为硫酸软骨素及硫酸乙酰肝素.CD44肽链的N端可结合透明质酸,故CD44也被视为透明质酸的受体.
CD44的功能包括: ①与透明质酸、纤粘连蛋白及胶原结合,介导细胞与细胞外基质之间的粘附;②参与细胞对透明质酸的摄取及降解;③参与淋巴细胞归巢;④参与T细胞的活化;⑤促进细胞迁移.
CD44在很多种肿瘤细胞的表达比相应正常组织为高,并与肿瘤细胞的成瘤性、侵袭性及淋巴结转移性有关.
细胞连接有哪几种类型?各有何功能?
细胞连接有紧密连接、粘着连接、间隙连接。紧密连接是细胞质膜上,紧密连接蛋白(门蛋白)形成分支的链索条,与相邻的细胞质膜上的链索条对应结合,将细胞间隙封闭。
锚定连接:通过中间纤维(桥粒、半桥粒)或微丝(粘着带和粘着斑)将相邻细胞或细胞与基质连接在一起,以形成坚挺有序的细胞群体、组织与器官。
通讯连接:包括间隙连接和化学突触,是通过在细胞之间的代谢偶联、信号传导等过程中起重要作用的连接方式。
细胞表面的特化结构,或特化区域,两个细胞通过这种结构连接起来。细胞的特化区涉及细胞外基质蛋白、跨膜蛋白、胞质溶胶蛋白、细胞骨架蛋白等。从功能上看,细胞连接将同类细胞连接成组织,并同相邻组织的细胞保持相对稳定。
细胞连接的类型和特点
1、游离面
①细胞表面(cell surface):又称细胞衣(cell coat),为一薄层绒状的复合糖,是细胞膜向外延伸的糖链部分,具有粘着、保护、物质交换及识别等功能.
②微绒毛(microvillus) 是细胞膜和细胞质共同突向腔面的细小指状突起,内部可见纵行的由肌动蛋白构成的微丝,与胞质内肌球蛋白相互作用,可使微绒毛伸长和缩短.微绒毛的作用是增加细胞游离面的表面积.
③纤毛(cillium) 是细胞顶端伸向腔面的突起,比微绒毛粗且长,内部为9+2微管结构,微管间相互滑动产生纤毛有节律的同步摆动.
2、
①紧密连接(tight junction):又称闭锁小带,位于单层柱状细胞之间,呈箍状环绕细胞顶端,相邻细胞膜外层呈网格状融合,细胞间隙消失.未融合处,有10-15nm宽的间隙.闭锁小带除有机械连接作用外,还有效地封闭了相邻细胞的顶部,防止细胞间隙中的物质溢出,也阻止大分子物质进入组织内.
②中间连接(intermediate junction):又称粘着小带,直接位于紧密连接下方,呈带状环绕细胞顶端,相邻细胞膜间宽约15-20nm,其中充以丝状物.在中间连接的胞质侧,可见电子致密层,有很多来自于终末网的细丝附着此处.中间连接能使终末网绷紧,保持细胞形状,与细胞收缩及松弛密切相关.
③桥粒(desmosome):又称粘着斑.呈圆盘状,位于细胞之间,连接处的细胞间隙约20-30nm,其中充满丝状物,并在中间密集交叉组成致密的中间线.细胞膜的胞质面有电子致密物质形成的附着板,胞质内的张力丝深入附着板,复而折回胞质.桥粒是上皮细胞间较为牢固的连接,故多见于易受机械刺激或摩擦部位的复层扁平上皮.
④缝隙连接(gap junction):又称通讯连接,呈斑状,分布于上皮细胞、肌细胞、神经细胞及骨细胞之间.连接处的相邻细胞膜紧密相贴,仅留有2-3nm的间隙.相邻两个细胞膜间有许多对应等距离的连接点,连接点是有细胞膜内六个亚单位蛋白颗粒围成直径1.5nm的小管,两侧小管互相接通,成为细胞间的交通管道.缝隙连接可供细胞互相交换某些小分子物质和离子,以传递化学信息.连接电阻也低,便于传递电冲动.
3、基底面
①基膜(basement membrane):又称基底膜,为上皮基底面与深部结绨组织间的薄膜,是由糖胺多糖和蛋白质构成的均质状膜,有支持和连接作用,还是半透膜,有利于上皮细胞与深部结缔组织进行物质交换.
② 质膜内褶(plasma membrane infolding):位于上皮细胞基底部,由细胞膜向细胞质内陷而形成,褶内有线粒体.质膜内褶可括大细胞基底部的表面积,有利于水和电解质的迅速转运.
(你直接把功能加到特殊组织后边就可以了.比如说质膜内褶的功能是有利于水和电解质的迅速运转就可以了啊.因为时间关系我就不多说了,你自己可以总结一下,很简单的.不要总是要别人来帮助你自己总结,自己也可以努力一下的.很简单的啊!)
以上就是关于细胞与细胞之间的连接有哪些方式,常见的细胞连接方式有哪几种的全部内容,以及细胞与细胞之间的连接有哪些方式的相关内容,希望能够帮到您。
版权声明:本文来自用户投稿,不代表【推酷网】立场,本平台所发表的文章、图片属于原权利人所有,因客观原因,或会存在不当使用的情况,非恶意侵犯原权利人相关权益,敬请相关权利人谅解并与我们联系(邮箱:350149276@qq.com)我们将及时处理,共同维护良好的网络创作环境。
大家都在看

柯南用绳子高空救小兰哪一集,柯南里那几集柯南救出小兰的
综合百科柯南用绳子高空救小兰哪一集1、柯南用绳子高空救小兰是《通往天国的倒计时这一集。2、剧情简介:小兰困在该大楼而没逃出来,空中走廊被爆炸的威力给炸断,但又必须救出小兰,因此柯南利用他的滑板飞越这天际到爆炸的大楼里,成功地将小兰给救出,但走廊炸断了,滑板也无法让两人成功地飞越这天际,小

妖精的尾巴莉莎娜第几集复活了
综合百科妖精的尾巴莉莎娜第几集复活了1、第95集。2、莉莎娜是在妖精的尾巴登场的人物,被暴走的哥哥艾尔夫曼重伤,随后在姐姐米拉的怀中消失。后来夏在另一个世界中与其相遇,但并未与其相认。最后随着逆转的超空间魔法——灵魂,回到马格诺利亚。3、角色介绍:日本动漫《妖精的尾巴》出现的角色,莉莎娜

拖欠工程款纠纷的起诉程序怎么走,拖欠工程款纠纷起诉程序怎么走法院
综合百科本文目录1.拖欠工程款纠纷起诉程序怎么走法院2.拖欠工程款最快最直接的解决电话3.到法院起诉拖欠工程款流程4.2023拖欠工程款起诉流程及费用是多少拖欠工程款纠纷起诉程序怎么走法院拖欠工程款纠纷起诉程序是:1、准确选择被告,选择发包人、承担连带责任保证担保方式的任何当事人;2、证

黑妞卡丁车怎么获得,跑跑卡丁车手游黑妞黑色喷漆怎么获得
综合百科黑妞卡丁车怎么获得1、根据最新版本的公告显示,这辆车将会在13号发起团购活动,参与团购的玩家将最低只用12元入手这辆史诗车。2、不过在之前的公告中对于这台车的登场预告却是定在了17号,所以有可能是13号开售17号才结束并发货吧。3、这台车目前除了是跑道具的而且应该算史诗级别以外其
多糖是什么 有什么用,什么是多糖
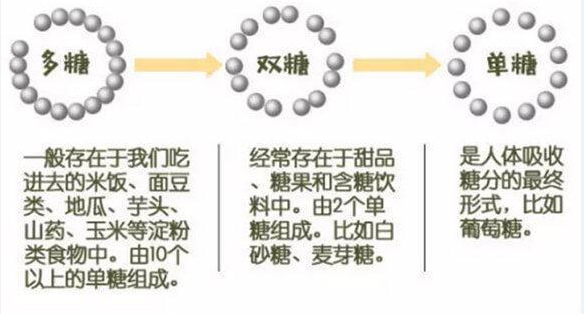
综合百科本文目录1.什么是多糖2.石斛多糖的作用是什么3.多糖的作用4.什么是多糖,多糖对人体有什么作用什么是多糖多糖是由单糖连接而成的多聚物,人们对它的研究最早可追溯至 1936年Dr.Shear对多糖抗肿瘤活性的发现。至20世纪50年代,一些真菌多糖和高等植物多糖被陆续发现具有明显的

怎么样做三色糙米饭
综合百科怎么样做三色糙米饭1、三色糙米100克,温水(浸泡)适量,盐少许,水(煮饭)150克左右,食用油1-2滴。2、准备制作食材。3、轻轻淘洗糙米3-4回,倒去浮上来的米和杂质,用30度左右的温水浸泡16小时,浸泡的水量刚刚没过糙米即可。4、水里可加少许盐以防细菌滋生,每5-6个小时换

如何让微信不显示忙线,微信不能显示对方正在输入
综合百科如何让微信不显示忙线微信没有设不设置忙线一说,如果有显示忙线一般是网络不佳或者对方通话被占线,只能等网络状况恢复或者等对方通话完毕。微信(wechat)是腾讯公司于2011年1月21日推出的一个为智能终端提供即时通讯服务的免费社交程序,微信支持跨通信运营商、跨操作系统平台通过网络

9年8月30日生肖运势如何
综合百科19年8月30日生肖运势如何1、生肖(鼠)心情愉悦,灵感不断,得到认可。2、生肖(牛)心态良好,他人相助,爱情运佳。3、生肖(虎)贵人助力,多多赞美,适合聚会。4、生肖(兔)贵人助力,化险为夷,事业轻松。5、生肖(龙)心态良好,他人相助,爱情运佳。6、生肖(蛇)压力较大,效率下降

发面用酒怎么发,用酒怎么发面做馒头
综合百科本文目录1.用酒怎么发面做馒头2.啤酒怎么发面做馒头3.怎么用酒发面做包子4.怎么用米酒发面蒸馒头?用酒怎么发面做馒头用酒发面是先将温水倒入盆子里,温度为35℃~40℃。然后倒入米酒、啤酒,再加入一勺白糖,之后搅拌均匀。再把面粉倒入盆子里,然后放入10克酵母粉,5克无铝泡打粉,迅

兔子产后如何护理,兔子生完小兔子以后要注意什么
综合百科兔子产后如何护理1、母兔分娩后,会跳出产箱找水喝。这时,应将产仔箱取出,清点仔兔,扔掉死胎、弱胎及污物,称重记数,并换上新鲜垫草。2、如母兔产仔过多或乳汁不足,可进行适当的调整。将过多的仔兔转移到产仔较少而乳汁又充足的哺乳母兔那里。将转移的仔兔身上涂以寄养母兔的乳汁或该母兔所生仔

苹果手机iphone x怎么样正确充电,苹果手机如何正确充电 寿命长
综合百科本文目录1.苹果手机如何正确充电 寿命长2.iphoneX有无线充电功能吗3.新苹果手机充电的正确方法是什么4.教你正确给苹果手机充电的四大方法视频苹果手机如何正确充电 寿命长1、及时充电:iPhone的电量低于20%时便会进行提示,电池显示处也会从绿色变成红色,这种时候最好要及

罗汉松种子几天能发芽,罗汉松种子多少天发芽
综合百科罗汉松种子几天能发芽一、几天能发芽罗汉松的种子在种植时若是新鲜的,种下后大概十天左右就能发芽。此外,种植前最好先进行催芽处理,这样成活率才能更高,且发芽时间也能缩短。二、怎么催芽催芽的时候要先把种子放在水中浸泡,水用白开水就可以,水的温度最好是和室内的温度相近,种子要全部泡在水里





