乙醇能使蛋白质变性
发布:小编
乙醇能使蛋白质变性吗?
能。
因为乙醇具有很强的渗透力,能够钻入细菌内部,使菌体蛋白质凝固,造成细菌因失去活性而死亡。
蛋白质变性是受物理或化学因素的影响,改变其分子内部结构和性质的作用。
蛋白质变性原因变性作用是蛋白质受物理或化学因素的影响,改变其分子内部结构和性质的作用。
一般认为蛋白质的二级结构和三级结构有了改变或遭到破坏,都是变性的结果。
能使蛋白质变性的化学方法有加强酸、强碱、重金属盐、尿素、丙酮等;能使蛋白质变性的物理方法有加热(高温)、紫外线及X射线照射、超声波、剧烈振荡或搅拌等。
蛋白质蛋白质是由多种氨基酸通过肽键构成的高分子化合物,在蛋白质分子中各氨基酸通过肽键及二硫键结合成具有一定顺序的肽链称为一级结构;蛋白质的同一多肽链中的氨基和酰基之间可以形成氢键或肽链间形成氢键,使得这一多肽链的主链具有一定的有规则构象,包括α-螺旋、β-折叠、β-转角和Ω-环等,这些称为蛋白质的二级结构;肽链在二级结构的基础上进一步盘曲折叠,形成一个完整的空间构象,称为三级结构;多条肽链通过非共价键聚集而成的空间结构称为四级结构,其中一条肽链叫一个亚基。
乙醇能使多肽变性
乙醇(酒精)具有很强的渗透力,能够钻入细菌内部,使菌体蛋白质(多肽组成)凝固(化学上叫做变性),造成细菌因失去活性而死亡。
酒精分子有两个末端,一端是憎水的(-C2H5),可以破坏蛋白质内部憎水基团之间的吸引力;一端是亲水的(-0H),但它难以破坏蛋白质外部的亲水基团之间的吸引力。
另一方面,水分子虽然可以松弛蛋白质亲水基团之间的吸引力,但它即使钻进细菌内部,也无法破坏其蛋白质中憎水基团之间的吸引力。
所以,纯酒精或水都不足以使细菌内的蛋白质变性,只有酒精和水共同存在,同时使保持蛋白质几何形状的各种吸引力松弛,蛋白质才会失去生理活性。因此,只有一定浓度的酒精溶液,才能达到良好的消毒杀菌目的。
酒精使蛋白质变性的原理是什么
蛋白质变性是蛋白质受到了物理或化学等因素的影响,改变了其分子内部结构,从而使其性质和功能发生了部分或者全部的变化,主要是氢键和离子键被破坏。
乙醇可以提供自己的羟基或羰基上的氢或氧去形成氢键,从而破坏了蛋白质中原有的氢键,使蛋白质变性。
另一方面是由于乙醇加入水中使溶剂介电常数降低,增加了相反电荷的吸引力,另一方面是因为这些有机溶剂是强亲水试剂,争夺蛋白质分子表面的水化水,破坏蛋白质胶体分子表面的水化层而使蛋白质分子聚集沉淀。
乙醇能降低介电常数的原理
酒精引起蛋白质沉淀的原因一方面是由于其加入水中使溶剂介电常数降低,增加了相反电荷的吸引力,另一方面是因酒精是强亲水试剂,争夺蛋白质分子表面的水化水,破坏蛋白质胶体分子表面的水化层而使分子聚集沉淀。
一定浓度的酒精才可以使蛋白质变性(比如医院用的75%的乙醇消毒液),并不是所有浓度的酒精都可以使蛋白质变性,有些浓度的酒精只会使蛋白质沉淀析出而已。
蛋白质变性的四种方法
强酸强碱重金属盐和尿素
在热、酸、碱、重金属盐、紫外线等作作用下,蛋白质会发生性质上的改变而凝结起来。这种凝结是不可逆的,不能再使它们恢复成原来的蛋白质。蛋白质的这种变化叫做变性,蛋白质变性之后,紫外吸收,化学活性以及粘度都会上升,变得容易水解,但溶解度会下降。
蛋白质变性后,就失去了原有的可溶性,也就失去了它们生理上的作用,因此蛋白质的变性凝固是个不可逆过程。
少量的盐(如硫酸铵、硫酸钠等)能促进蛋白质的溶解。如果向蛋白质水溶液中加入浓的无机盐溶液,可使蛋白质的溶解度降低,而从溶液中析出,这种作用叫做盐析。
这样盐析出的蛋白质仍旧可以溶解在水中,而不影响原来蛋白质的性质,因此盐析是个可逆过程。利用这个性质,采用分段盐析方法可以分离提纯蛋白质。
以上就是关于乙醇能使蛋白质变性的全部内容,以及乙醇能使蛋白质变性吗?的相关内容,希望能够帮到您。
版权声明:本文来自用户投稿,不代表【推酷网】立场,本平台所发表的文章、图片属于原权利人所有,因客观原因,或会存在不当使用的情况,非恶意侵犯原权利人相关权益,敬请相关权利人谅解并与我们联系(邮箱:350149276@qq.com)我们将及时处理,共同维护良好的网络创作环境。
大家都在看

将进酒怎么读
综合百科将进酒怎么读1、读法:[qiāngjìnjiǔ]将进酒。2、《将进酒》的语境中,“将”读“qiāng”是无疑的,在古汉语中,这个“将”意为“邀请”。说通俗点,“将进酒”就是“请你再喝一杯酒”。3、由于在现代汉语中,“将”的多个古义已经失去,一般指代“将要”的意思,所以很多人容易读

电笔显示12v36v是漏电吗?,电笔在多少伏的电压下就会发亮点笔上显示2v36v是啥意思
综合百科本文目录1.电笔测试显示出⚡️2 36 55 0这个数值属于漏电2.电笔显示12 36 55 110 220是什么意思3.电笔多少电压会亮灯4.电笔显示12是漏电吗电笔测试显示出⚡️2 36 55 0这个数值属于漏电1、你这是数字显示的感应测电笔;2、测电笔是测量不出漏电的;3、

宝马哪国产的车,宝马是哪国产的车型
综合百科本文目录1.宝马是哪国产的车型2.宝马是哪国产的车型3.宝马中国产地在哪里4.宝马是哪国产的宝马是哪国产的车型宝马是德国产的。宝马的正式汉字全称为巴伐利亚发动机制造厂股份有限公司,是一个闻名于世界的豪华汽车品牌,总部位于巴伐利亚的慕尼黑。宝马经常被称为Bimmer,品牌在中国大陆

宝马玻璃日期怎么看出来,宝马车玻璃怎么看生产日期13Q
综合百科宝马玻璃日期怎么看出来1、你仔细看挡风玻璃上的商标(一般在左下角或右下角)。有一串字符:“****。09****。”2、一般情况下当中的那个数字就代表玻璃的生产年份。而“*”则代表季度,“。”就代表月份:“**..09”则代表该档风玻璃是09年5月份生产的。3、也有数字前后全是“

蛋酥的做法 这样做就很好吃,鸡蛋酥怎么做好吃又简单
综合百科本文目录1.鸡蛋酥怎么做好吃又简单2.怎样做鸡蛋酥小零食3.一品蛋酥的制作方法窍门4.蛋酥怎么制作视频鸡蛋酥怎么做好吃又简单1、用料:鸡蛋一斤、白糖2两、麦芽糖1两。2、把1斤鸡蛋打在碗里,加2两白糖搅拌均匀。3、麦芽糖倒入碗中,隔水大火加热2分钟,凝固的麦芽糖就能融化了。4、倒
按农历一年四季怎么分,一年四季怎么划分月份英语
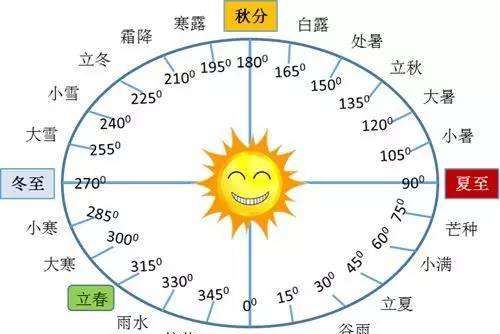
综合百科按农历一年四季怎么分我国传统的四季农历划分方法,是以二十四节气中的四立作为四季的始点,以二分和二至作为中点的。如春季以立春为起点,春分为中点,立夏为终点。夏季以立夏为起点,夏至为中点,立秋为终点。秋季以立秋为起点,秋分为中点,立冬为终点。冬季以立冬为起点,冬至为中点,立春为终点。

死亡之海是哪一个沙漠,中国死亡之海是哪个沙漠
综合百科本文目录1.中国死亡之海是哪个沙漠2.中国死亡之海是哪个沙漠3.死亡之海指的是哪个沙漠4.号称死亡之海的沙漠是哪个中国死亡之海是哪个沙漠塔克拉玛干沙漠塔克拉玛干在维吾尔语意思为走得进,出不来,西方探险家斯坦因在100年前将其称为死亡之海。塔克拉玛干沙漠是新疆南疆的塔里木盆地中心,

暑伏适合吃什么食物,暑伏吃什么 吃了有什么好处
综合百科暑伏吃什么 吃了有什么好处1、藕作为一种养生食物,有清热凉血,通便止泻、健脾开胃,益血生肌,止血散瘀之功效,三伏天多吃些藕,对健康好处多多。2、俗语中常有“鱼生火、肉生痰”的说法,那么鱼和肉这些容易“上火”的食物,夏天自然应该少吃。不过,黄鳝却是个例外。黄鳝肉嫩鲜美,营养丰富,滋

朦胧诗派的特点,朦胧诗派的代表诗人有哪些人
综合百科本文目录1.朦胧诗派的代表诗人有哪些人2.朦胧诗的特点是什么举例说明3.举例说明朦胧诗的艺术特征4.简述朦胧诗的艺术特征朦胧诗派的代表诗人有哪些人致橡树舒婷朦胧诗代表人物我如果爱你——/绝不学攀援的凌霄花,/借你的高枝炫耀自己;/我如果爱你——/绝不学痴情的鸟儿,/为绿荫重复单调

机动车没年审怎么处罚,机动车没有年审上路怎么处罚
综合百科本文目录1.机动车没有年审上路怎么处罚2.机动车逾期未年检怎样处罚 二个月3.车辆没有年审怎么处罚规定4.新车超过两年没年检怎么办机动车没有年审上路怎么处罚有一些车主因为忘了自己车子的检测时间,使得应该年审的时候没有去检查,这个也是车主有可能会碰到的问题,那么遇到汽车没有年审会有

相互理解包容的语录,相互理解包容励志语录
综合百科相互理解包容的语录每天提醒自己,不要忘记理想,不要忘记目标;每天提醒自己,不要忘记学习,不要忘记看书;每天提醒自己,不要忘记包容,不要忘却善心;每天提醒自己,不要忘记身体,不要忘记锻炼;每天提醒自己,不要忘记美丽,不要忘记快乐;每天提醒自己,不要忘记爸妈,不要忘记亲人。度量如海涵

如何处理危机公关,如何做好危机公关?
综合百科如何处理危机公关1、充分传播。当事组织向媒体、公众、消费者及一切关注事件的人们,提供一切可能的沟通办法,如新闻发布会、媒体现场采访、网络互动、热线电话、公开信、广告、短信等等传播方式和手段,保证社会大众的知情权。2、承担责任。当事组织利用这样那样的传播手段和工具,不是要辩解、争论








